Kilka lat temu mocno rozprzestrzeniła się wiedza na temat powszechności występowania mutacji w genie MTHFR oraz potencjalnych zagrożeniach, jakie się z nim wiążą. Jako że temat wyglądał interesująco (a genetyka zaiste jest niezwykle interesująca), a badanie było stosunkowo łatwe do zrobienia, ogromna ilość osób zaczęła się diagnozować i szukać interpretacji swoich wyników we wszystkich możliwych miejscach, po czym wdrażać suplementację witaminami B.
Czym jest metylacja?
Metylacja jest procesem biochemicznym polegającym na transferze grupy metylowej (CH3) pomiędzy różnymi cząsteczkami. Reakcji metylacji zachodzi u nas bardzo dużo, a uczestniczą one między innymi w regulacji genów, produkcji neuroprzekaźników, „aktywacji” niektórych witamin, regulacji poziomu homocysteiny, czy też syntezy osłonek mielinowych na neuronach. Często pojęcie metylacji odnosi się konkretnie do metylacji DNA, ponieważ za sprawą tego procesu organizm reguluje aktywność genów. Odpowiadają za to enzymy — metylazy DNA, które dołączają grupy metylowe do zasad azotowych nukleotydów, najczęściej do cytozyny. W ten sposób geny są włączane lub wyłączane, co fachowo jest nazywane ekspresją genów.
Popularnym terminem są zaburzenia metylacji. Zjawisko to polega na zaburzeniu pracy enzymu reduktazy metylenotetrahydrofolianu, co skutkuje zmniejszoną dostępnością aktywnej formy witaminy B9 i S-adenozylometiony w ustroju.
Za co odpowiada gen MTHFR?
Gen MTHFR koduje syntezę enzymu o tym samym akronimie – reduktazy metylenotetrahydrofolianu. U ludzi MTHFR znajduje się w lokalizacji p36.3 chromosomu 1 i jest łańcuchem składającym się z 656 aminokwasów. Enzym MTHFR uczestniczy w cyklu kwasu foliowego i ma prostą funkcję: katalizuje redukcję 5,10-metylenotetrahydrofolianu (5,10-Methylene-THF) do 5-metylotetrahydrofolianu (5-MTHF). 5-MTHF (inaczej metylofolian) jest bardzo ważnym kofaktorem w ludzkim organizmie i gdy przez zbyt niską dostępność enzymu zmniejsza się jego ilość, pojawiają się problemy. Najbardziej doniosłą jego funkcją jest asysta w pracy enzymu syntazy metioniny, który konwertuje potencjalnie szkodliwą homocysteinę w metioninę (proces remetylacji homocysteiny), przywracając ją do obiegu cyklu metioninowego. Następnie metionina jest przekształcana w SAMe (s-adenozylometioninę) i ta substancja jest kluczowa w całej układance, ponieważ to ona jest głównym donorem grup metylowych do procesów metylacji, które wymieniałem wcześniej, czyli metylacja DNA, synteza neuroprzekaźników itp. Jeśli MTHFR jest niesprawny, to pośrednio wpływa to na zmniejszenie dostępności SAMe i akumulacji homocysteiny. Sprawny MTHFR umożliwia utrzymanie prawidłowego balansu pomiędzy tymi molekułami i utrzymywania ciągłości cyklu metioniny.

Mutacja MTHFR
Wyżej padł taki termin jak mutacja genu MTHFR, jednak od razu muszę go lekko sprostować. Zazwyczaj tak się określa to zjawisko, ale termin ten nie jest do końca poprawny, ponieważ w przypadku tego genu należy mówić raczej o jego polimorfizmie, niż mutacji. Różnica pomiędzy mutacją i polimorfizmem polega głównie na częstotliwości występowania. Określenie „mutacja MTHFR” już na tyle mocno się utarło, że po wyjaśnieniu, o co z tym chodzi, pozwolę sobie dalej używać tego potocznego terminu, mając nadzieję, że się na mnie za to nie obrazisz 😉
Mutacja genetyczna występuje niezwykle rzadko i zazwyczaj jej skutki są bardzo poważne. Te dwie cechy są ze sobą poniekąd powiązane, ponieważ poważne konsekwencje zdrowotne zazwyczaj oznaczają zmniejszoną przeżywalność, mocno skróconą długość życia lub brak zdolności do prokreacji, co za sprawą mechanizmu selekcji naturalnej sprawia, że mutacja nie może osiągać dużych statystyk w społeczeństwie. Mutacje konkretnego genu zazwyczaj dotyczą mniej niż 1% społeczeństwa.
Polimorfizm za to nie wpływa na ciężkie problemy i często można z takim polimorfizmem żyć, nawet o nim nie wiedząc. W ten sposób ludzie z polimorfizmami normalnie żyją i się rozmnażają, przekazując swój profil genetyczny potomstwu i zwiększając udział danego wariantu genu w społeczeństwie. Statystyki takich polimorfizmów mogą sięgać nawet kilkudziesięciu procent. Prawdę mówiąc, polimorfizm genetyczny często jest bardziej osobniczą cechą niż zaburzeniem i tak jest też w przypadku polimorfizmów genu MTHFR.
Popularne polimorfizmy
Polimorfizmy mogą występować heterozygotyczne lub homozygotyczne, co oznacza, że defekt został przekazany przez jednego lub obojga rodziców. Wariant hetero oznacza, że tylko jeden z dwóch alleli jest zmieniony i jest to wariant łagodny. Polimorfizm homozygotyczny natomiast wskazuje na zmianę obu alleli, co już może mocno wpływać na funkcjonowanie genu. Polimorfizmy homozygotyczne są poważniejsze, ale też wielokrotnie rzadsze.
Istnieje wiele możliwych polimorfizmów MTHFR, z czego znanych jest na pewno 14, jednak wyszczególnione zostały dwa, które mają największą częstość występowania i znaczenie kliniczne – tylko one mają udokumentowany wpływ na zmniejszenie aktywności enzymu.
MTHFR 677C>T
Ten polimorfizm oznacza, że w sekwencji genu MTHFR w 222 pozycji łańcucha zamiast alaniny występuje walina. Ten wariant, szczególnie homozygotyczny, uznawany jest za sporą predyspozycję do rozwoju chorób układu krążenia. Polimorfizm ten oznaczany jest obecnie również jako MTHFR 665C>T. Polimorfizm heterozygotyczny oznacza 67% aktywności enzymatycznej MTHFR, natomiast homozygotyczny jedynie 25%, co już jest poważnym osłabieniem enzymu.
MTHFR 1298A>C
Zmiana kwasu glutaminowego na alaninę w 429 pozycji łańcucha białkowego. Zdaniem genetyków ma mniejszy wpływ na zdrowie układu krążenia i ma mniejszą wartość diagnostyczną w kardiologii, jednak również wpływa na wzrost poziomu homocysteiny. Polimorfizm heterozygotyczny oznacza 83% aktywności enzymatycznej MTHFR, natomiast homozygotyczny 61%. Widać więc sporą różnicę w stosunku do wariantu 677C>T.
Jednoczesne występowanie heterozygotycznych polimorfizmów 677C>T i 1298A>C redukuje aktywność enzymatyczną do 48%.
Częstotliwość występowania
Częstotliwość występowania polimorfizmów genu MTHFR jest zależna od rasy i pochodzenia. Polimorfizmy są bardzo częste u rasy białej i kaukaskiej, mogą występować nawet u 50% populacji. Za to rzadko są wykrywane u przedstawicieli rasy czarnej – 22% ogółem, przy czym homozygotyczne 677C>T u tylko 2%.
Poniższa mapka przedstawia częstość występowania homozygoty 677C>T w różnych populacjach.
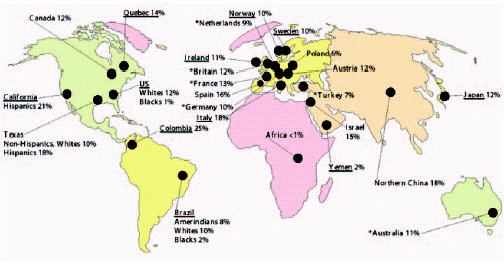
Objawy mutacji genu MTHFR
Sama mutacja nie powoduje żadnych objawów, ponieważ nie zawsze oznacza ona, że w organizmie pojawiają się niekorzystne zmiany w znaczącym stopniu. Niekiedy współwystępowanie innych predyspozycji i prowadzenie zdrowego trybu życia może spowodować kompletny brak efektów polimorfizmu. Natomiast faktyczne objawy, jeśli się pojawią, to mogą być wynikiem potencjalnych konsekwencji niedoboru metylofolianu i hiperhomocysteinemii.
Choroby układu krążenia
Najbardziej specyficznym, biochemicznym objawem zaburzeń MTHFR jest znaczny wzrost homocysteiny. Homocysteina jest prozapalna i zwiększa stres oksydacyjny w śródbłonku. Niestety przewlekle utrzymujące się wysokie stężenia homocysteiny znacznie zwiększają ryzyko chorób układu krążenia, w tym miażdżycy.
Choroby psychiatryczne i neurologiczne
Są doniesienia, że poziom homocysteiny jest odwrotnie skorelowany z ryzykiem depresji. Homocysteina efektywnie przekracza barierę krew-mózg i uważana jest za neurotoksynę, m.in. ze względu na podnoszenie aktywności receptorów NMDA i AMPA układu glutaminianu. Powoduje nadmierny napływ jonów wapnia do komórek i indukuje uszkodzenia mitochondriów, a to zaburza proces produkcji ATP i ogranicza dostępność energii do pracy neuronów. W krótkiej perspektywie nadmierna stymulacja układu glutaminianu może się objawiać np. niepokojem, drażliwością i gorszym samopoczuciem, a w dłuższej perspektywie różnego rodzaju neurodegeneracją, w tym zwiększeniem ryzyka choroby Alzheimera. Istnieją przesłanki wiążące polimorfizmy MTHFR z predyspozycją do rozwoju różnych schorzeń psychiatrycznych, jednak nadal jest to temat do dalszych badań, ponieważ nie ma twardych wniosków. Badania dotyczą głównie wpływu na schizofrenię, chorobę dwubiegunową, ADHD i zaburzenia ze spektrum autyzmu.
Wpływ na ciążę
Badanie tego genu często wykonywane jest też u kobiet po kilkukrotnych poronieniach. Niekiedy mutacja MTHFR utrudnia donoszenie ciąży do końca, ponieważ aktywny folian ma krytyczne znaczenie w przebiegu rozwoju płodu. Oficjalne stanowisko Polskiego Towarzystwa Genetyki Człowieka i Polskiego Towarzystwa Ginekologów i Położników z 2017 roku jednak nie jest przychylne badaniom genu MTHFR, w wielu przypadkach nie uznają wartości predykcyjnej w diagnostyce przeprowadzanej pod kątem przyczyn nawracających poronień, ryzyka urodzenia się dziecka z wadą rozwojową układu nerwowego, aberracjami chromosomowymi (w tym z zespołem Downa), ryzyka wystąpienia zakrzepicy, udarów niedokrwiennych mózgu, choroby wieńcowej, chorób afektywnych, zaburzeń rozwoju psychosomatycznego i niepełnosprawności intelektualnej lub niektórych chorób nowotworowych.
Pozostałe
Nadmiar homocysteiny i niedobór folianów ciągną za sobą też inne, niepożądane następstwa. Chroniczna hiperhomocysteinemia może potencjalnie doprowadzać do zaburzeń pracy nerek, układu trawiennego i problemów z kośćmi.
Badanie MTHFR
Pewnie zastanawiasz się, gdzie zbadać gen MTHFR? Jest już sporo laboratoriów, które podejmują się tego badania komercyjnie. Można udać się osobiście do odpowiedniego laboratorium albo zamówić zestaw do samodzielnego pobrania materiału. Takim zestawem pobiera się wymaz śliny z jamy ustnej. Jest to bardzo prosta czynność – należy otrzymanym sterylnym patyczkiem potrzeć o wewnętrzną ścianę policzka, najlepiej z rana jeszcze przed jedzeniem i myciem zębów. Następnie zamyka się patyczek w również otrzymanym, specjalnym opakowaniu i odsyła paczką do laboratorium z wypełnionymi i podpisanymi dokumentami, jakie są wymagane przez laboratorium wykonujące badanie.
Przykładowe laboratoria, które mają badanie genu MTHFR w ofercie:
- Diagnostyka
- TestDNA
- Euroimmun DNA
Cena badania genu MTHFR mieści się w zakresie 150-300 zł, w zależności od laboratorium. Czas oczekiwania na wynik powinien oscylować w okolicach 14 dni.
Badania pomocnicze
Poza badaniem samego polimorfizmu wykonuje się też badania markerów z krwi, które pozwalają ocenić realny wpływ genu na biochemię, opracować strategię naprawczą i monitorować postępy.
Najważniejsze jest badanie homocysteiny we krwi. Homocysteina jest funkcjonalnym markerem dostępności aktywnych form witamin z grupy B, a w szczególności B6, B9 i B12. Jej poziom pozwala też realnie ocenić ryzyko zdrowotne. Jeśli wiesz, że masz polimorfizm MTHFR, to badanie homocysteiny jest mocno wskazane. Jeśli wyjdą nieprawidłowości, to warto później sprawdzać ponownie efekty, jednak nie szybciej niż po upływie 3 miesięcy.
Często wykonywane są też badania kwasu foliowego i witaminy B12 we krwi. Przy polimorfizmach często poziom kwasu foliowego wychodzi za wysoko, ponieważ nie może być z odpowiednią wydajnością konwertowany do aktywnej formy. Badanie witaminy B12 natomiast nie ma tak dużej wartości diagnostycznej, jakiej byśmy oczekiwali. Jednym z powodów jest to, że witamina B12 jest kumulowana w wątrobie, dlatego poziom we krwi nie musi pokazywać dokładnie ogólnego nasycenia organizmu. Za funkcjonalne markery nasycenia witaminą B12 uznaje się kwas metylomalonowy (MMA) i holotranskobalaminę II (Holo-TC).
Podsumowanie
Polimorfizmy genu MTHFR są bardzo powszechne, jednak nie jest to poważna przypadłość i na pewno nie jest powodem do paniki. Jeśli tylko masz diagnozę i świadomość istnienia takiego polimorfizmu, wystarczy, że podejmiesz bardzo proste działania, jak wdrożenie odpowiedniej suplementacji i wykonywanie okresowych badań, by trzymać rękę na pulsie.
Osobiście jestem posiadaczem homozygotycznego polimorfizmu MTHFR 677TT, który jest tym najgorszym i najbardziej znaczącym klinicznie, zwiększającym ryzyko miażdżycy. Nie wywołuje to u mnie obaw, ponieważ wiem, co z tym robić i mam sytuację pod kontrolą – suplementację stosuję od wielu lat i poziom homocysteiny mam ciągle satysfakcjonujący. Jedyne co mocno zwróciło moją uwagę i uważam, że jest warte zanotowania to, że po odebraniu wyniku badania i włączeniu do suplementacji aktywnego B-Kompleksu, odnotowałem bardzo szybką i zauważalną poprawę samopoczucia 🙂
Źródła:
- Lin Wan et al. „Methylenetetrahydrofolate reductase and psychiatric diseases” Transl Psychiatry. 2018; 8: 242.
- A. McCaddon et al. „Functional vitamin B12 deficiency and Alzheimer disease” Neurology May 2002, 58 (9) 1395-1399;
- Henrieta Škovierová et al. „The Molecular and Cellular Effect of Homocysteine Metabolism Imbalance on Human Health” Int J Mol Sci. 2016 Oct; 17(10): 1733.
- Hanna Moczulska i in. „Stanowisko ekspertów Polskiego Towarzystwa Genetyki
Człowieka i Polskiego Towarzystwa Ginekologów i Położników w sprawie zlecania i interpretacji wyników badań pod kątem wariantów genetycznych w genie MTHFR” Ginekologia i Perinatologia Praktyczna 2017 tom 2, nr 5, strony 234–238 - Daniel Leclerc, Sahar Sibani, and Rima Rozen „Molecular Biology of Methylenetetrahydrofolate Reductase (MTHFR) and Overview of Mutations/Polymorphisms” Madame Curie Bioscience Database
Wojciech Nowosada
Powiązane artykuły
1 Komentarz
Dodaj komentarz Anuluj pisanie odpowiedzi
Ta strona używa Akismet do redukcji spamu. Dowiedz się, w jaki sposób przetwarzane są dane Twoich komentarzy.

Wartościowy artykuł. Właśnie zdiagnozowano u mnie MTHFR_1298A>C układ homozygotyczny. Powodem wykonania badania jest przewlekła leukopenia, bez zdiagnozowanej przyczyny. Badania B12, kw.foliowy – w normie. Wkrótce badanie homocysteiny. Mam pytanie: czy tego typu mutacja może powodować zmiany w budowie naczyń krwionośnych na etapie płodowym? Urodziłam się z niewykształconą żyłą ramienną, wytworzyło się krążenie oboczne, które w jakiś sposób dotlenia rękę i jest w 80% sprawna. Nie mniej, splątanie naczyń w okolicach łokcia naciska na dwa nerwy i wywołuje okresowe bardzo silne bóle. Najgorszy stan występuje podczas ciąży w I.trymestrze. Od lat szukam specjalisty, który potrafiłby rzeczowo odpowiedzieć na pytanie, dlaczego ten ból nasila się właśnie w ciąży. Życie z tym bólem i problemem jest do zaakceptowania, ale już wizja trzech miesięcy ciągłego bólu do łez skutecznie zniechęca do dalszego macierzyństwa. Być może pisząc ten artykuł dotarłeś do materiałów, które mogłyby mnie zainteresować. Z góry dzięki.